
|
PIT00568 Экзоцитоз Экзоцито́з (от др.-греч. ἔξω — «вне, снаружи» + κύτος — «клетка») — механизм клеточных выделений: - у эукариот клеточный процесс, при котором внутриклеточные везикулы (мембранные пузырьки) сливаются с внешней клеточной мембраной. При экзоцитозе содержимое секреторных везикул (экзоцитозных пузырьков) выделяется наружу, а их мембрана сливается с клеточной мембраной. Практически все макромолекулярные соединения (белки, пептидные гормоны и др.) выделяются из клетки этим способом. - у прокариот везикулярный механизм экзоцитоза не встречается: у них экзоцитозом называют встраивание белков в клеточную мембрану (или в наружную мембрану у грамотрицательных бактерий), выделение белков из клетки во внешнюю среду или в периплазматическое пространство. Экзоцитоз может выполнять три основные задачи: • доставка на клеточную мембрану липидов, необходимых для роста клетки; • высвобождение различных соединений из клетки, например, токсичных продуктов метаболизма или сигнальных молекул (гормонов или нейромедиаторов); • доставка на клеточную мембрану функциональных мембранных белков, таких как рецепторы или белки-транспортёры. При этом часть белка, которая была направлена внутрь секреторной везикулы, оказывается выступающей на наружной поверхности клетки. 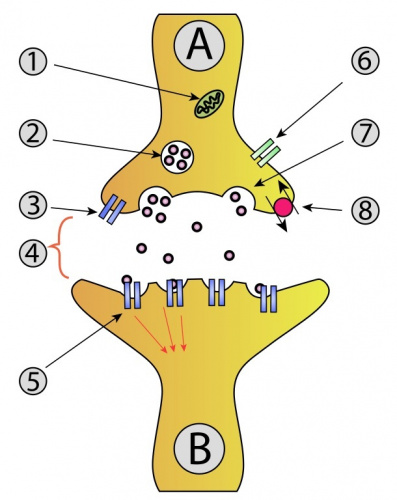 Экзоцитоз в синапсе - передача сигнала от нейрона А к нейрону B. 1. Митохондрия. 2. Синаптическая везикула с нейромедиатором. 3. Ауторецептор. 4. Синапс с выделенным нейромедиатором. 5. Постсинаптический рецептор, активируемый нейромедиатором. 6. Кальциевый канал. 7. Экзоцитоз-везикулы. 8. Рециркуляция нейромедиатора. У эукариот различают два типа экзоцитоза: 1. Кальций-независимый конститутивный экзоцитоз встречается практически во всех эукариотических клетках. Это необходимый процесс для построения внеклеточного матрикса и доставки белков на внешнюю клеточную мембрану. При этом секреторные везикулы доставляются к поверхности клетки и сливаются с наружной мембраной по мере их образования. 2. Кальций-зависимый неконститутивный экзоцитоз встречается, например, в химических синапсах или клетках, вырабатывающих макромолекулярные гормоны. Этот экзоцитоз служит, например, для выделения нейромедиаторов. При этом типе экзоцитоза секреторные пузырьки накапливаются в клетке, а процесс их высвобождения запускается по определённому сигналу, опосредованному быстрым повышением концентрации ионов кальция в цитозоле клетки. В пресинаптических мембранах процесс осуществляется специальным кальций-зависимым белковым комплексом SNARE. Различают следующие этапы экзоцитоза: • Транспортировка везикулы от места синтеза и формирования (аппарат Гольджи) до места доставки осуществляется моторными белками вдоль актиновых филаментов либо микротрубочек цитоскелета. Этот этап может потребовать перемещения секретируемого материала на значительное расстояние, как, например, в нейроне. Когда везикула достигает места секреции, она входит в контакт со специфическими удерживающими факторами клеточной мембраны. • Удержание доставленной везикулы обеспечивается относительно слабыми связями на расстоянии более 25 нм и может служить, например, для концентрирования синаптических везикул около пресинаптической мембраны. • Стыковка везикулы с мембраной является непосредственным продолжением первой фазы доставки, когда мембрана везикулы входит в близкий контакт с мембраной клетки (5-10 нм). Это включает прочное соединение белковых компонентов обеих мембран, вызванным внутримолекулярными перестановками, и предваряет формирования SNARE комплекса. • Стимуляция (прайминг) везикулы фактически соответствует образованию особого SNARE комплекса между двумя мембранами и осуществляется только в случае нейронального экзоцитоза. Этот этап включает процессы молекулярных перестановок и АТФ-зависимые модификации белков и липидов, происходящие непосредственно до слияния мембран в ответ на подъём уровня свободного кальция. Этот кальций-зависимый процесс необходим для контролируемого быстрого выброса нейромедиатора и отсутствует в случае конститутивного экзоцитоза. • Слияние мембраны везикулы с мембраной клетки приводит к высвобождению, или выбросу, содержания секретируемой везикулы во внеклеточное пространство и объединению липидного бислоя везикулы с внешней мембраной. В случае синаптического выброса процесс слияния, так же как и стимуляция, осуществляется SNARE комплексом. 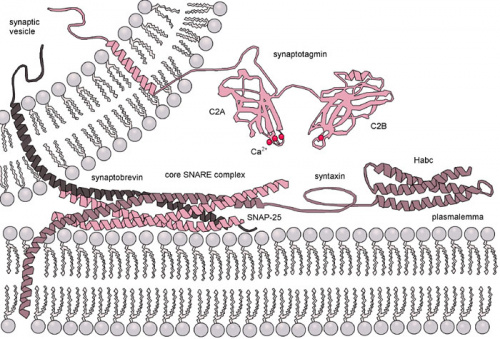 Молекулярная машина экзоцитозного высвобождения нейромедиатора в синапс. SNARE комплекс формируется за счёт образования четырёхспиральной сцепки между синаптобревином, синтаксином и SNAP-25. Синаптотагмин служит кальциевым сенсором и внутренним регулятором комплексообразования. SNARE (от англ. soluble NSF attachment receptor) — большая группа белков, осуществляющих слияние внутриклеточных транспортных везикул с клеточной мембраной (экзоцитоз) или органеллой-мишенью, такой как лизосома. Насчитывается около 60 белков SNARE. Белки группы делятся на две функциональные категории: везикулярные белки (v-SNARE) и белки принимающей органеллы (t-SNARE). Новая структурная классификация подразделяет группу на R-SNARE и Q-SNARE. Наиболее изучены белки, которые выполняют доставку синаптических везикул к пресинаптической мембране и их слияние. Эти белки являются мишенями опасных бактериальных токсинов ботулизма и столбняка. Белки SNARE являются небольшими, но широко-представленными мембранными белками. Несмотря на большую разницу в структуре и размере эти белки объединяет наличие одного и того же цитозольного домена из 60—70 аминокислот, называемого SNARE motif (или SNARE домен), способного к образованию обратимой, но прочной четырёхспиральной сцепки. Такой метастабильный транс-SNARE комплекс включает синтаксин 1 и SNAP-25, находящиеся на клеточной мембране, и синаптобревин на поверхности доставляемой пресинаптической везикулы. Синтаксин и синаптобревин связаны с мембраной С-конечным фрагментом и предоставляют по одной альфа-спирали в четырёхспиральную сцепку комплекса. SNAP-25 заякорен на мембране за счёт пальмитоильных ацильных цепей и обеспечивает две оставшиеся альфа-спирали. {Lang2008} Lang, Thorsten, and Reinhard Jahn. Core proteins of the secretory machinery (Основные белки секреторного аппарата) // Pharmacology of neurotransmitter release # 184, 107-127 (2008). doi 10.1007/978-3-540-74805-2_5 Аннотация. Члены семейств Rab, SM- и SNARE-белков играют ключевую роль на всех стадиях доставки внутриклеточных мембран. В то время как SM- и SNARE-белки становятся непосредственно вовлеченными в реакцию слияния на поздней стадии, Rab и их эффекторы опосредуют предшествующие этапы, такие как отпочкование пузырьков, доставка, прикрепление и транспорт. Экзоцитоз синаптических везикул и регулируемых секреторных гранул является одним из наиболее изученных событий слияния и включает изоформы Rab3 Rab3A-D, белок SM munc18-1 и синтаксин 1A, SNAP-25 и синаптобревин 2 SNARE. Т. е. синтаксин 1А и SNAP-25 на пресинаптической мембране образуют комплекс с синаптобревином 2, ассоциированным с синаптической везикулой. По мере формирования комплекса противоположные мембраны плотно стягиваются друг с другом, усиливая реакцию слияния. Munc18-1 необходим для регулируемого экзоцитоза и взаимодействует только с синтаксином 1A или с комплексами SNARE, указывая на роль munc18-1 в контроле реакции сборки SNARE. По сравнению с другими стадиями внутриклеточного слияния, в синапсе развились особые приспособления, обеспечивающие жесткую регуляцию и высокую скорость оборота мембраны, необходимые для синаптической передачи. Слияние синаптических пузырьков запускается внутриклеточным вторичным мессенджером кальция, при этом члены семейства белков синаптотагмина являются первыми кандидатами на связывание притока кальция со слиянием в быстрой фазе экзоцитоза. Чтобы компенсировать массовое включение синаптических пузырьков в плазматическую мембрану во время экзоцитоза, в синапсе развились специальные приспособления к эндоцитарным механизмам, обеспечивающие эффективную рециркуляцию пузырьков. Cited by 163 Peter Belobrov 21 May 2023 19:38
© International Open Laboratory for Advanced Science and Technology — MOLPIT, 2009–2026
|