
|
PIT00642 Регенерация периферических нервов Перспектива. Периферическая нервная система и микробиота кишечника: Новые данные о расширении знаний о механизмах, позволяющие разработать инновационные стратегии регенерации периферических нервов [1]. Микробиота кишечника: организм человека населён разнообразным и сложным микробным сообществом, включающим бактерии, вирусы, археи и одноклеточные эукариоты, которое играет ключевую роль в поддержании здоровья человека. Микробиота критически важна для множества функций, включая метаболизм хозяина, физиологию, поддержание целостности эпителия кишечника, питание и иммунную функцию, что позволяет ей называться «жизненно важным органом» (Guinane and Cotter, 2013). Значительная часть этих микробов находится в желудочно-кишечном тракте: было подсчитано, что кишечник человека содержит более 100 триллионов микробных клеток, при этом микробиом содержит примерно в 100 раз больше генов, чем человеческий геном (примерно 3 миллиона генов в микробиоме человека и около 23 000 генов в геноме человека) (Rinninella et al., 2019). Доминирующими типами кишечных микробов являются Firmicutes, Bacteroidetes, Actinobacteria, Proteobacteria, Fusobacteria и Verrucomicrobia, причем Firmicutes и Bacteroidetes вместе составляют 90% кишечной микробиоты. В типе Firmicutes (грамположительные бактерии, составляющие примерно 46–58% от общего числа бактерий кишечника) род Clostridium составляет 95%, тогда как в типе Bacteroidetes (грамотрицательные бактерии, составляющие примерно 30–40% от общего числа бактерий) преобладают роды Bacteroides и Prevotella. Тип Actinobacteria менее распространён (3–7%) и представлен в основном родом Bifidobacterium (Rinninella et al., 2019). Каждый человек имеет уникальный профиль кишечной микробиоты, характеризующийся определённым сочетанием видов бактерий, на формирование которого влияют меж- и внутрииндивидуальные различия. Состав кишечной микробиоты может меняться на протяжении жизни под влиянием ряда факторов, включая географическое положение, культурные привычки, питание, физические нагрузки, образ жизни, стресс, применение или злоупотребление антибиотиками, возраст, пол, прогрессирующее ухудшение физиологических показателей и заболевания (Rinninella et al., 2019; Hou et al., 2022). Все больше данных подтверждают двунаправленную или даже многонаправленную связь между кишечной микробиотой и органами за пределами кишечника через нервные, эндокринные, гуморальные, иммунологические и метаболические пути. Следовательно, нарушения тонкого баланса хозяина и микробиома, известные как дисбактериоз, могут не только вызывать проблемы, связанные с кишечником, но и играть значительную роль в патогенезе заболеваний других органов, включая сердечно-сосудистую или дыхательную системы, заболевания головного мозга, рак и другие (Hou et al., 2022). Механизмы, посредством которых микробиота может влиять на другие органы или центральную и периферическую нервную систему (PNS), еще предстоит тщательно изучить. В настоящее время предлагаемые гипотезы включают системные эффекты высвобождения кишечных веществ, такие как секреция био- или нейроактивных метаболитов, полученных от микробиоты (Kern et al., 2024). Кроме того, взаимодействие между микробиотой кишечника и иммунной системой играет решающую роль в развитии мозга и патогенезе неврологических заболеваний (Fung et al., 2017). Ось «кишечник-периферическая нервная система»: В последние годы взаимодействие между микробиотой кишечника и энтеральной нервной системой – ветвью PNS, расположенной в стенке желудочно-кишечного тракта – было описано как при физиологических, так и при патологических состояниях (Calabrò et al., 2023). Энтеральная нервная система играет важную роль во многих физиологических процессах в желудочно-кишечном тракте и в значительной степени независима от центральной нервной системы. Её функции включают регуляцию, например, эпителиальной секреции, обмена жидкости через эпителий слизистой оболочки, барьерной функции, кровотока в кишечнике, иммунной системы и моторики кишечника. Энтеральная нервная система напрямую подвергается воздействию и взаимодействует с микробиотой кишечника и метаболитами. Появляющиеся данные свидетельствуют о том, что микробиота кишечника может оказывать существенное влияние на развитие и функцию как энтеральных нейронов, так и глиальных клеток (Calabrò et al., 2023). Совсем недавно мы исследовали потенциальное взаимодействие между микробиотой кишечника и соматической нервной системой — компонентом PNS, ответственным за произвольный контроль движений тела скелетными мышцами и за передачу соматосенсорной информации с периферии тела в мозг. 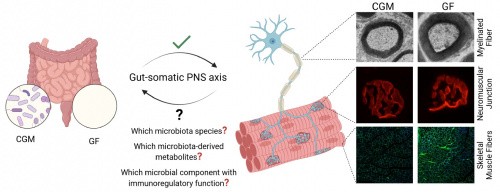 Схематическая иллюстрация, демонстрирующая текущие и будущие исследования влияния состава кишечной микробиоты на PNS и её органы-мишени. В первую очередь необходимо выявить различия между крайностями, такими как сложная кишечная микробиота и стерильные условия (как показано слева). Недавние исследования были сосредоточены на стереоморфометрии аксонов периферических нервов и двигательной ткани-мишени (как показано справа). Дальнейшие исследования будут сосредоточены на выявлении специфических составов кишечной микробиоты, в частности, связанных с ними метаболитов или микробных компонентов с иммунорегуляторными функциями (например, липополисахаридов, бактериальных капсульных полисахаридов и пептидогликана), чтобы определить, какие виды микробиоты оказывают наиболее значимое влияние на ось кишечник-соматическая система-PNS. Создано с помощью BioRender.com. CGM - сложная кишечная микробиота; GF - стерильная; PNS - периферическая нервная система. [1]. Ronchi, Giulia, Matilde Cescon, Giovanna Gambarotta, and Kirsten Haastert-Talini. Peripheral nervous system and gut microbiota: emerging evidence on increased mechanistic understanding to reveal innovative strategies for peripheral nerve regeneration // Neural Regeneration Research 21 (4), 1560-1561 (2026). doi 10.4103/NRR.NRR-D-24-01310 Peter Belobrov 28 Sep 2025 00:50
© International Open Laboratory for Advanced Science and Technology — MOLPIT, 2009–2026
|